КОНТРОЛЬНАЯ РАБОТА ПО ХИМИИ
8 КЛАСС
КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
ВАРИАНТ 4
1. Определите степени окисления элементов в соединениях: H2SeO4, BaSeO3, SeBr2, SeO3, Se, K2Se. Какие из этих соединений являются за счет селена:
а) только окислителями
б) только восстановителями
в) проявляют двойственность окислительно-восстановительных свойств?
2. Составьте уравнения реакций:
а) H3PO4 → H4P2O7 + H2O
б) H2O2 → H2O + O2
в) Cu + HNO3 → Cu(NO3)2 + H2O + NO
г) KNO3 → KNO2 + O2
д) K2Cr2O7 + KOH → K2CrO4 + H2O
Какие из реакций являются окислительно-восстановительными? Составьте, где необходимо, электронный баланс.
3. Для нитрата свинца (II) приведите по две реакции, протекающие
а) с изменением степеней окисления
б) без изменения степеней окисления.
Приведите для указанных вами реакций, где это необходимо, электронный баланс и ионные уравнения реакций.
4. В трех пробирках находятся растворы: Ba(NO3)2, Cu(NO3)2, NaNO3. Какие реактивы потребуются, чтобы определить, в какой пробирке какой раствор находится? Какие признаки химических реакций наблюдаются? Приведите уравнения реакций.
5. Углерод массой 10 г, содержащий 4% примесей, сожгли в избытке кислорода. Полученный газ пропустили через избыток раствора гидроксида бария. Определите массу выпавшего осадка.
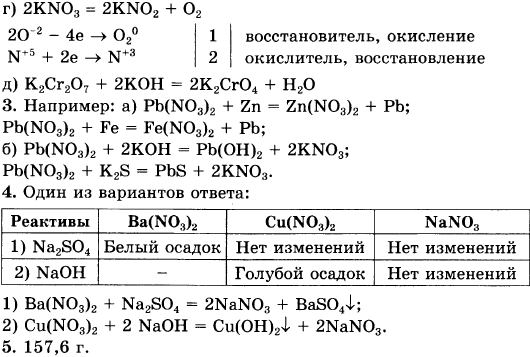
Решения и ответы:

ВСЕ КОНТРОЛЬНЫЕ РАБОТЫ ЗА КУРС ХИМИИ 8 КЛАССА


